Vai trò bổ trợ và làm giảm nồng độ IL-22 huyết thanh của Meriva® trên bệnh nhân bị vẩy nến
Bệnh vẩy nến là một bệnh mãn tính thường gặp do tăng sinh tế bào hoặc viêm. Các tổn thương thường thấy ở da, móng và khớp, ảnh hưởng đến khoảng 2% dân số thế giới, làm suy giảm chất lượng cuộc sống của người mắc bệnh. Với hoạt tính chống viêm và một số tính chất ưu điểm như độ an toàn và khả năng dung nạp cao đã được chứng minh trong nhiều nghiên cứu in vivo và in vitro, Curcumin trở thành một tác nhân đầy hứa hẹn cho việc điều trị bệnh vẩy nến. Cơ chế hoạt động của Curcumin có thể thông qua việc tương tác với các con đường bệnh sinh chính của bệnh như ức chế nhân tố hạt nhân kappa B (NF-κB), tăng sinh keratinocyte, ức chế phosphorylase kinase (PhK) và sự hình thành mạch. Việc sử dụng Curcumin trong điều trị bệnh vẩy nến chủ yếu dựa trên các báo cáo giai thoại, có rất ít nghiên cứu khảo sát hiệu quả của nó trong điều trị bệnh vẩy nến đã được thực hiện. Năm 2015, một nhóm tác giả thuộc Khoa Da liễu, Khoa Phẫu thuật và Y học, Đại học Florence, Ý đã thực hiện một nghiên cứu lâm sàng nhằm đánh giá vai trò của Curcumin trong bệnh vẩy nến. Nghiên cứu sử dụng Meriva® - curcumin dạng phytosome với lecithin- như một biện pháp bổ trợ để điều trị bệnh vẩy nến nhẹ đến vừa. Nghiên cứu so sánh hiệu quả của việc điều trị vẩy nến bằng methylprednisolone aceponate 0.1% dùng tại chỗ kết hợp uống Meriva® và methylprednisolone aceponate 0.1% dùng tại chỗ kết hợp uống giả dược. Ngoài ra, nghiên cứu còn điều tra ảnh hưởng của phương pháp điều trị như vậy tới nồng độ IL-7 và IL-22 trong huyết thanh, đây là các interleukin đại diện cho các cytokines được tiết ra từ T helper 17 và T helper 22, 2 yếu tố đóng vai trò quan trọng trọng của quá trình sinh bệnh.
-3.jpg)
Hình 1: Cấấu trúc phân tử của Meriva®
Đối tượng nghiên cứu là những bệnh nhân có triệu chứng về mặt mô học của bệnh vẩy nến từ nhẹ đến trung bình, Điểm PASI < 10 (thang điểm đánh giá bệnh vẩy nến dựa trên mức độ đỏ da, dày da, vảy da và diện tích từng phần cơ thể bị tổn thương). Tiêu chuẩn loại trừ là: Bệnh nhân < 18 tuổi, bệnh nhân bị guttate, erythrodermic, hoặc mụn mủ vẩy nến, cũng như viêm khớp vẩy nến; bệnh nhân sử dụng các phương pháp trị liệu toàn thân cho bệnh vẩy nến trong vòng 3 tháng trước ngày số 0 hoặc bất cứ lúc nào trong quá trình nghiên cứu; bệnh nhân sử dụng phương pháp điều trị tại chỗ hoặc quang trị liệu cho bệnh vẩy nến trong vòng 1 tháng trước khi nghiên cứu hoặc bất cứ lúc nào trong quá trình nghiên cứu; phụ nữ có thai hoặc cho con bú; phụ nữ trong độ tuổi sinh đẻ không sử dụng biện pháp tránh thai đáng tin cậy; bệnh nhân có các bất thường có ý nghĩa lâm sàng khi thử nghiệm sàng lọc, hoặc có khó chịu đáng kể. Người tham gia đăng ký được yêu cầu để tránh tiếp xúc kéo dài với ánh sáng mặt trời hoặc tia cực tím và để ngưng sử dụng các chất làm mềm trong vòng 24 giờ trước mỗi lần nghiên cứu. Nghiên cứu đã được phê duyệt bởi hội đồng thẩm định viện của bệnh viện Ospedale Piero Palagi (Florence, Ý); tất cả các bệnh nhân đều đã đồng ý bằng văn bản.
Tất cả bệnh nhân được hướng dẫn uống 2 viên x 2 lần một ngày, mỗi viên chứa 500mg Meriva® (Indena SpA, Milan), với tổng liều hàng ngày là 2 g. Đây là một thử nghiệm lâm sàng giai đoạn III, liều đơn, mù đội, ngẫu nhiên có đối chứng trên bệnh nhân vẩy nến mạn tính mảng bám. Nghiên cứu được thực hiện tại Khoa Phẫu thuật và Dịch tễ Y khoa, Khoa da liễu (Đại học Florence, Ý), bao gồm một giai đoạn sàng lọc, một thời gian cơ sở để đánh giá điểm PASI và bắt đầu điều trị, thời gian điều trị kéo dài 12 tuần, và 4 tuần theo dõi. Bệnh nhân được phân ngẫu nhiên theo tỷ lệ 1: 1 vào 2 nhóm. Nhóm 1: Sử dụng thuốc mỡ methylprednisolone aceponate 0,1% bôi tại chỗ (mỗi ngày một lần trên các thương tổn) kết hợp uống 2g Meriva® mỗi ngày (2 viên 500 mg, hai lần một ngày). Nhóm 2: Sử dụng thuốc mỡ methylprednisolone aceponate 0,1% (bôi một lần mỗi ngày tại vị trí thương tổn) kết hợp với uống giả dược (2 viên giống nhau về kích thước, hình thức, và màu sắc, hai lần mỗi ngày). Liều lượng thuốc của tất cả các bệnh nhân đều được phân tích an toàn. Dữ liệu an toàn thu được bằng cách phỏng vấn bệnh nhân và khám nghiệm lâm sàng được thực hiện bởi bác sỹ tại tất cả các chuyến thăm nghiên cứu.
Bệnh nhân được đánh giá điểm PASI tại các thời điểm T0, T4, T8, T12 và T16 sau khi đã sử dụng Meriva® và giả dược . Tiêu chuẩn hiệu quả thứ cấp bao gồm PASI 50, PASI 75, PASI 90, và PASI 100 (Giảm 50%, 75%, 90%, và 100%, tương ứng, trong điểm PASI ban đầu). Mỗi thời điểm được đánh giá bằng phương pháp so sánh giữa tỷ lệ bệnh nhân đạt tiêu chuẩn đó trong các nhóm. Tại thời điểm tuần 0 (T0) và tuần 12 (T12), bệnh nhân được lấy mẫu huyết thanh để đo nồng độ IL-17 và IL-22. Mẫu máu lấy từ cả hai nhóm được đem ly tâm trong 20 phút ở 10.000xg (5417R, Eppendorf, Hamburg, Đức). Sau đó mẫu huyết thanh được chia thành các aliquots nhỏ và lưu trữ ở -80°C. Bộ dụng cụ thử nghiệm miễn dịch (ELISA) được sử dụng để xác định IL-17 và IL-22 trong huyết thanh (R & D Systems, Minneapolis, MN, USA), theo chỉ dẫn của nhà sản xuất.
Phân tích thống kê hiệu quả lâm sàng của Meriva® sử dụng phương pháp kiểm định Wilcoxon để so sánh sự khác nhau về lâm sàng trước và sau điều trị, giữa nhóm 1 (Meriva®) và nhóm 2 (Giả dược). Dữ liệu IL-17 và IL-22 được phân tích bằng Student’s T-test. Sự khác biệt có ý nghĩa thống kê khi p<0.05.
Kết quả:
- Có 85 bệnh nhân tham gia sàng lọc, trong đó 63 người đã được ghi danh và được chọn ngẫu nhiên vào một trong hai nhóm. Trong số 22 người không tham gia, có 4 người bị loại trừ vì PASI > 10; 9 người đã sử dụng phương pháp điều trị tại chỗ trong vòng 30 ngày trước ngày số 0; 5 người đã sử dụng phương pháp điều trị toàn thân trong vòng 3 tháng trước ngày 0 và 4 bệnh nhân mắc đồng thời arthropathy.
Có 31 bệnh nhân đã được ghi danh vào nhóm 1 (nhóm sử dụng Meriva®) và 32 bệnh nhân ghi danh vào nhóm 2 (giả dược). Trong số 31 bệnh nhân được ghi danh vào nhóm 1, có 25 người đã hoàn thành thử nghiệm đến tuần thứ 16 và 6 người không hoàn thành; 2 người đã bị dừng lại trước tuần 12 do thiếu hiệu quả, 1 người do tác dụng không mong muốn (tiêu chảy) và 3 người bị mất theo dõi. Trong số 32 người được ghi danh vào nhóm 2, có 24 người đã hoàn thành thử nghiệm đến tuần thứ 16 và 8 người không hoàn thành; 6 người đã bị dừng lại trước tuần 12 vì thiếu hiệu quả hoặc tình trạng bệnh vẩy nến xấu đi, 2 người do tác dụng không mong muốn (ban sần trên mặt, buồn nôn và hô hấp). Thông tin cơ sở về người tham gia được trình bày trong Bảng 1.
|
|
Meriva® (n=31) |
Giả dược (n=32) |
|
Giới tính |
14 nam, 17 nữ |
18 nam, 14 nữ |
|
Tuổi |
37 (19-62) |
41 (22-59) |
|
Chủng tộc |
30 da trắng, 1 Hispanic |
32 da trắng |
|
Tuổi khởi phát |
31 (14-54) |
35 (20-51) |
Bảng 1: Thông tin người tham gia thử nghiệm Meriva® so với giả dược
- Kết quả lâm sàng:
- Giá trị PASI trung bình tại thời điểm T0 là 5.6 [4.2-7.3] ở nhóm sử dụng Meriva® và 4.7 [3.8-5.8] ở nhóm giả dược. Tại thời điểm T12, giá trị PASI đều giảm đáng kể ở cả 2 nhóm - nhóm sử dụng Meriva® : PASI ở T12 = 1.3 [0,6-1,7], PASI T0 so với PASI T12: p <0,05; Nhóm giả dược: PASI ở T12 = 2,4 [1,4-3,0], PASI T0 so với PASI T12: p <0,05; Hình 2). Tuy nhiên, mức độ giảm giá trị PASI của những bệnh nhân được điều trị steroid tại chỗ kết hợp Meriva® (nhóm 1) lớn hơn ở những bệnh nhân điều trị steroid tại chỗ kết hợp giả dược (nhóm 2) (p<0.05). Sự suy giảm PASI vẫn được duy trì ở cả 2 nhóm tại thời điểm T16 (nhóm 1: PASI ở T16 = 1,4 [1,2-1,8], PASI T0 so với PASI T16: ???? <0,05; nhóm 2: PASI ở T16 = 2,5 [1.8-3.3], PASI T0 so với PASI T16: ???? <0,05; Hình 2). Tại thời điểm T16, độ giảm PASI ở nhóm 1 vẫn lớn hơn so với nhóm 2 (p
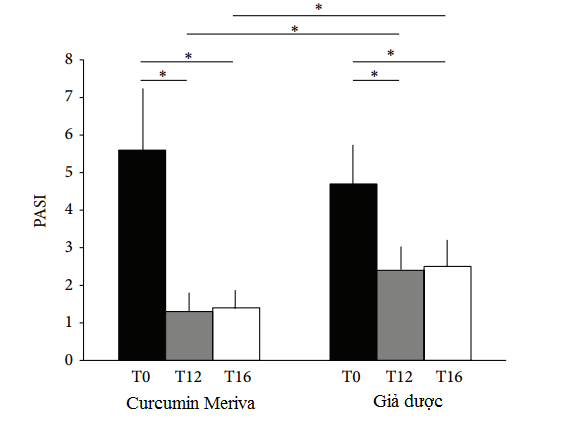
Hình 2: Giá trị PASI trung bình tại thời điểm T0, T12 và T16 của 2 nhóm sử dụng Meriva® so với giả dược
- Tại thời điểm T12, có 23 bệnh nhân ở nhóm sử dụng Meriva® (92%) và 13 bệnh nhân ở nhóm giả dược (54%) đạt được PASI 50; 12 bệnh nhân ở nhóm sử dụng Meriva® (48%) và 3 bệnh nhân ở nhóm giả dược (12%) đạt được PASI 75; 5 bệnh nhân ở nhóm sử dụng Meriva® ( 20%) và 1 bệnh nhân ở nhóm giả dược (4%) đạt được PASI 90%; và có 3 bệnh nhân ở nhóm sử dụng Meriva® (12%), 1 bệnh nhân ở nhóm giả dược (4%) đạt được PASI 100 (Bảng 2).
Tại thời điểm sau 4 tuần hoàn thành điều trị T16, có 22 bệnh nhân ở nhóm sử dụng Meriva® (88%) và 11 bệnh nhân ở nhóm giả dược (46%) vẫn duy trì PASI 50; 11 bệnh nhân ở nhóm sử dụng Meriva® (44%) và 2 bệnh nhân ở nhóm giả dược (8%) duy trì PASI 75; 2 bệnh nhân ở nhóm sử dụng Meriva® ( 8%) và 0 bệnh nhân ở nhóm giả dược (0%) duy trì PASI 90%; và có 1 bệnh nhân ở nhóm nhóm sử dụng Meriva® (4%), 0 bệnh nhân ở nhóm giả dược (0%) duy trì PASI 100 (Bảng 2).
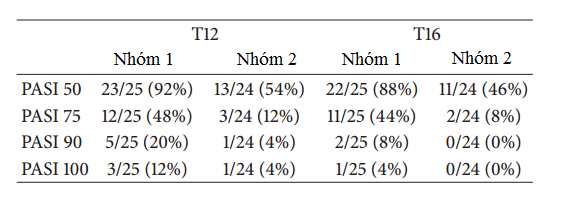
Bảng 2: Hiệu quả thứ cấp tại T12 và T16 ở nhóm Meriva® so với giả dược
- Về mức độ Cytokines trong huyết thanh: IL-17 và IL-22 được phát hiện ở tất cả bệnh nhân khi sử dụng Meriva® . Tại thời điểm T0, mức IL-17 ở cả 2 nhóm tương tự nhau, không có sự khác biệt đáng kể (32.3 ± 13.6 ở nhóm 1 và 30.7 ± 12.2 ở nhóm 2, Hình 3), Sau điều trị, tại thời điểm T12, sự thay đổi nồng độ IL-17 ở cả 2 nhóm đều không có sự khác biệt đáng kể (30.7 ± 10.9 ở nhóm 1 và 28.8 ± 12.9 ở nhóm 2, Hình 3). Cũng giống như IL-17, mức độ IL-22 ở cả hai nhóm tương tự nhau tại thời điểm T0 (35.2 ± 9.5 ở nhóm 1 và 32.9 ± 11 ở nhóm 2, Hình 3). Tuy nhiên, sau 12 tuần điều trị, bệnh nhân được điều trị với methylprednisolone aceponate tại chỗ kết hợp với Meriva® có sự giảm đáng kể IL-22 huyết thanh (21,1 ± 7,5, IL-22 ở T0 so với IL-22 ở T12: p <0,001), trong khi điều trị với methylprednisolone aceponate tại chỗ kết hợp với giả dược không ảnh hưởng đến mức độ IL-22 (28,8 ± 10; Hình 3)
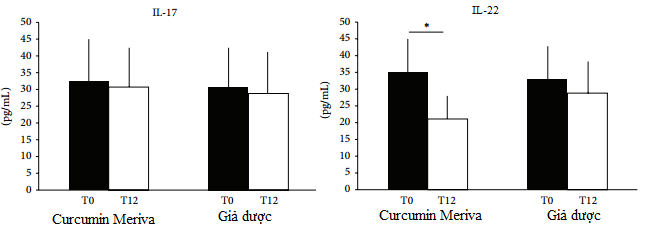 Hình 3: Các giá trị trung bình IL-17 và IL-22 tại (T0) và sau 12 tuần (T12) ở bệnh nhân điều trị bằng methylprednisolone tại chỗ + Meriva® (curcumin) hoặc điều trị bằng methylprednisolone tại chỗ + giả dược.
Hình 3: Các giá trị trung bình IL-17 và IL-22 tại (T0) và sau 12 tuần (T12) ở bệnh nhân điều trị bằng methylprednisolone tại chỗ + Meriva® (curcumin) hoặc điều trị bằng methylprednisolone tại chỗ + giả dược.
Từ những kết quả thu được sau thử nghiệm, có thể thấy sự kết hợp giữa thuốc mỡ bôi tại chỗ methylprednisolone aceponate 0,1% với Meriva® tốt hơn sự kết hợp giữa methylprednisolone aceponate 0,1% và giả dược trong điều trị bệnh vẩy nến. Trên thực tế, mặc dù cả hai phác đồ đều cho hiệu quả đáng kể nhưng bệnh nhân sử dụng cả steroid tại chỗ và Meriva® có sự giảm các giá trị PASI cao hơn đáng kể so với bệnh nhân sử dụng steroids tại chỗ kết hợp với giả dược.Hơn nữa, nhóm bệnh nhân có uống Meriva® đạt được PASI 50, PASI 75, PASI 90 và PASI 100 cao hơn so với nhóm uống giả dược, điều đó cho thấy Meriva® dạng uống có thể hữu ích trong điều trị bổ trợ bệnh vẩy nến.
Nguyên liệu Meriva® - Curcumin Phytosome hiện đang được phân phối bởi Công ty Cổ phần Dược phẩm Thiên Nguyên.
Chi tiết liên hệ Hotline CSKH 0947 805 345.
Thiên Nguyên - Đồng hành cùng Doanh nghiệp
Nguyên liệu ngành Dược, TPCN & TACN
Có thể bạn quan tâm: